Жирные кислоты ОМЕГА-3 и спортивные травмы. Возможная помощь при лечении?
Для лечения таких разных процессов как сужение бронхов, которое возникает при интенсивных аэробных нагрузках, или воспаление сухожилия, начинают использовать жирные кислоты Омега 3. На чем может быть основана новая диета? Имеет ли она научное обоснование?
На самом деле речь идет о воздействии на общий механизм указанных патологий, а именно воспаление. Воспаление в целом является положительным процессом, т.к. восстанавливает поврежденную ткань, тем не менее, при любом воспалительном процессе живые клетки разрушаются полиморфонуклеарными лимфоцитами, при этом макрофаги активизируют свободные радикалы, которые провоцируют разрушение ткани. Поэтому с определенного момента воспаление является нежелательным, в результате начинаем использовать противовоспалительные средства (стероидные или нестероидные).
Такие препараты задерживают синтез простагландинов (PG). Семейства простагландинов синтезируются из ненасыщенных жирных кислот почти во всех клетках. Их дневное синтезируемое количество равно приблизительно 1 мг, оказывает действие при небольших концентрациях и быстро дезактивируются в легких. При этом оказывается разнообразное действие: от сокращения гладких мышц и понижения кровяного давления до участия в воспалительных процессах. Все они являются производными 15-гидрокси-?13 (транс)-простановой кислоты.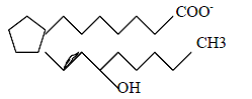
Итак, производные этих ненасыщенных кислот имеют разные свойства, поэтому PG, которые синтезируются из арахидоновой кислоты (АА) относятся к серии 2 и 4, т.е. те, которые участвуют в воспалительных реакциях и повышенной чувствительности. Производные эйкозапентаеновой кислоты (ЕРА), наоборот, относятся к серии 3 и 5 с небольшим или нулевым воспалительным действием и регулирующей функцией агрегации тромбоцитов.
Циклооксигеназа (СОХ) регулирует синтез простагландинов (PG). Были идентифицированы 2 изоформы: СОХ-1 и СОХ-2. СОХ-2 является прекурсором тромбоксана А2, простациклинов и PGD2, PGE2, PGF2alfa и т.д. СОХ-1 находится во многих клетках ткани, в то время как СОХ-2 отсутствует в них, хотя очень легко индуцируется в виде ответа на воспалительные воздействия. (Tapiero H et al 2002). (Рис. 1)
Теоретически диетическое использование заключается в уменьшении источника арахидоновой кислоты и увеличении Омега 3 (Connor WE 2001). Но для того, чтобы это возымело действие на практике, должны быть выполнены следующие условия:
- Потребленные жирные кислоты должны достичь мембран и мест, где происходят физиологические процессы.
- Должны измениться концентрации простагландинов и тромбоксан, вызывающих воспаление.
- Эта метаболическая гипотеза должна быть обоснована клиническими испытаниями (эксперименты на животных и людях).
Мы проверим выполняются ли эти условия. Для этого напомним метаболизм жирных кислот.
1. ХАРАКТЕРИСТИКИ ЛИПИДОВ
Липиды – это соединение биомолекул, общим свойством которых является гидрофобия. Липиды могут быть сложными и простыми, к последним относятся жирные кислоты, являющиеся органическими монокарбоксильными кислотами с линейной цепочкой, в которой число углеродных атомов составляет от 4 до 24, причем наиболее многочисленными являются цепочки с числом атомов от 14 до 22. Ненасыщенные кислоты имеют двойною связь (CН=СН), что можно отметить буквой С и нижними указателями m:n, при этом С – углерод, m – общее число атомов углерода и n – общее число атомов ненасыщенной связи (например, олеиновая кислота с 18 углеродами и только одной ненасыщенной связью будет иметь обозначение С18:1). Другое, более привычное обозначение – это название позиции двойной связи в пределах последних 7 атомов углерода в цепочке, считая от метилового конца цепи жирной кислоты (рис. 2) в позиции 3 (серия n3 или Омега 3) или позиции 6 (серия n6 или Омега 6) (линоленовая кислота представляет Омега 3, арахидоновая кислота - Омега 6). Таблицы I и II.
Переваривание жиров происходит в тонком кишечнике, где триглицериды, являющиеся компонентом жира пищи, под воздействием панкреатической липазы преобразуются в диглицериды, моноацилглицерины и жирные кислоты. Панкреатическая секреция содержит эстеразы, которые расщепляют фосфолипиды (энзим-катализатор – это фосфолипаза А2, который синтезируется в поджелудочной железе как проэнзим и активируется в кишечнике посредством трипсина).
Наш организм может синтезировать большинство жирных кислот из ацетилкоэнзима А, получаемого из углеводов, посредством мультиэнзиматического комплекса, именуемого синтаза жирных кислот (Рис. 3). Кроме того, имеются системы удлинения цепочки жирных кислот, которые позволяют увеличить число атомов углерода до 18 в случае насыщенных кислот и до 24 для ненасыщенных кислот, а также системы для введения двойных связей посредством десатураз жирных кислот. Тем не менее, нельзя ввести двойные связи в позиции после С9. Итак, некоторые наиболее важные для организма биомолекулы, такие как простагландины и тромбоксаны, являются производными жирных кислот, которые не могут синтезироваться организмом, и поэтому необходимо их потребление с пищей. (Таблица III).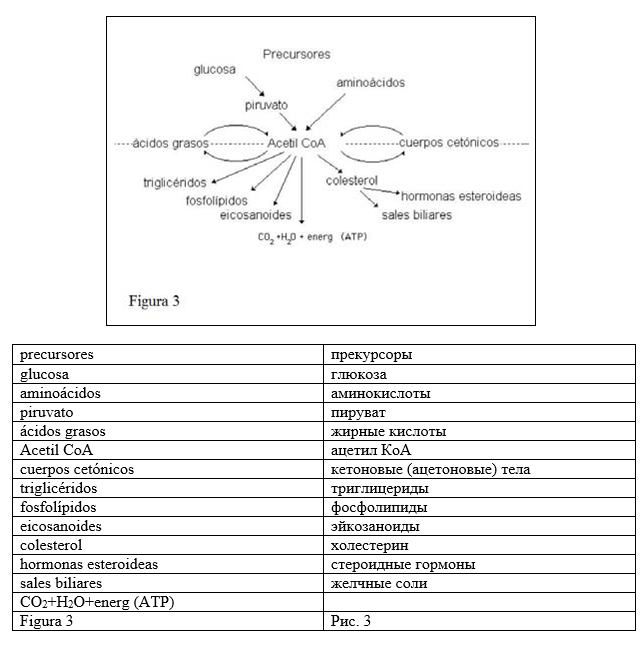
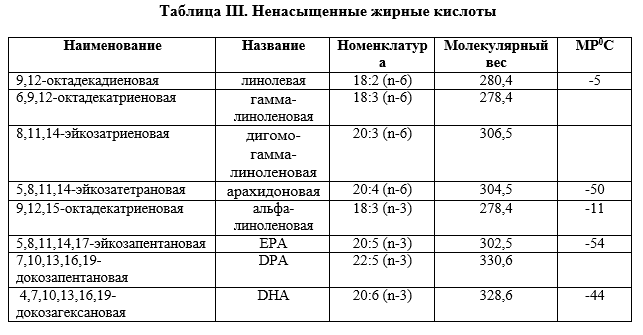
Человеческий организм может синтезировать жирные кислоты семейства Омега-9, но не может синтезировать жирные кислоты семейств Омега-6 и Омега-3. К этим кислотам относится линолевая, арахидоновая и линоленовая кислоты. Однако овощи могут синтезировать кислоты семейств Омега-6, а некоторые (особенно микроскопические морские водоросли) могут синтезировать кислоты семейства Омега-3. Например, рыбы накапливают кислоты Омега-6 и Омега-3 из потребляемого планктона.
Известно, что содержание и характеристики фосфолипидов, присутствующих в различных мембранах разных клеток организма, изменяется в зависимости от потребностей каждого органа. Таким образом, каждый фосфолипид, в зависимости от своей структуры, имеет определенные физико-химические свойства, которые он, являясь частью мембраны, передает ей. В зависимости от превалирующего компонента мембрана становится более или менее текучей, более или менее проницаемой относительно того или иного вещества, и ее движения будут более или менее простыми (Рис.4).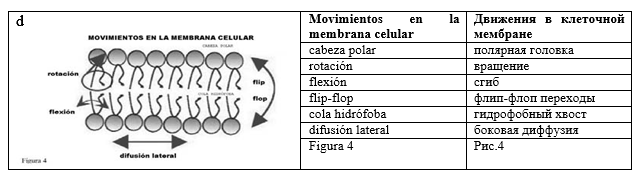
Поэтому следует отметить важность процентного содержания липидов, имеющихся в каждой мембране, причем этот процент генетически предопределен. Итак, в общих словах можем отметить, что генетический прогноз относительно конкретных жирных кислот, которые должны занимать определенную позицию в каждом фосфолипиде липидной мембраны, отсутствует, при этом имеются только общие сведения относительно их характеристик. Тот факт, что жирная кислота занимает ту или иную определенную позицию, в большей степени зависит от диеты.
Если диета оказывает важное значение на свойства мембран, ее серьезные изменения должны оказывать прямое воздействие на ряд патологий (ишемическая кардиомиопатия, диабет, ревматоидный артрит, болезнь Крона, астма, нефропатия IgA, депрессия и в целом большая часть воспалительных заболеваний). Для подтверждения этого просто следует провести библиографический поиск (Li D 2003).
2 – ИЗМЕНЕНИЯ В ПОТРЕБЛЕНИИ ЖИРОВ В ИНДУСТРИАЛЬНОМ ОБЩЕСТВЕ
Изменения в диете связаны с резкими переменами, которые претерпел наш вид: после тысяч лет охоты и собирательства стал вести сидячий образ жизни. Т.е. после выходы из определенной экологической ниши, расположенной на восточном побережье Африки, где питался рыбой, овощами, дикими животными и фруктами (питание богатое жирными кислотами Омега-3 (Crawford MA 1990)), мы стали потреблять откормленных на фермах животных, выращенные зерно и овощи, молочные и переработанные продукты (питание богатое жирными кислотами Омега-6 и насыщенными жирами). (Рис.5). Это стало резким изменением для вида, у которого не было времени адаптировать свою генетическую информацию, и который, следовательно, продолжает нуждаться в пище, богатой Омега-3 (Simopoulos AP et al. 2001).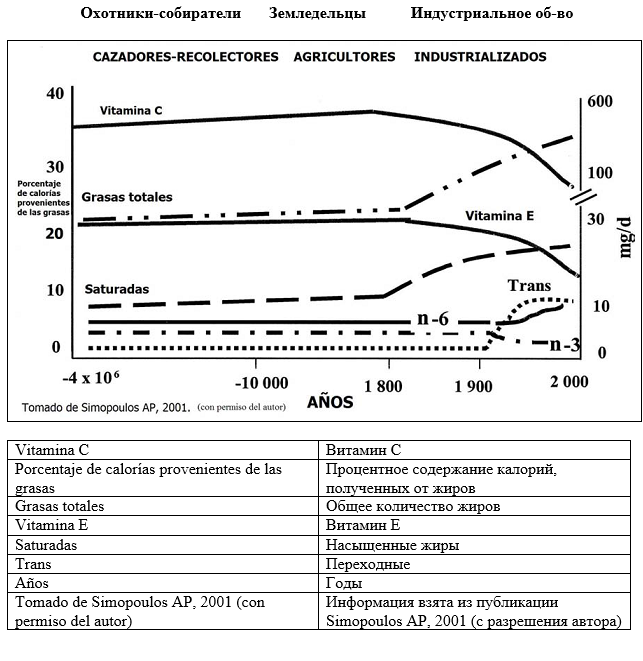
Наиболее понятный способ проверки данной гипотезы – исследование здоровья народа, который быстро перешел с палеолитического типа питания к питанию, которое приближено к диете любой индустриальной страны. Данный вопрос был детально проанализирован на основании тщательного исследования публикаций в указателях медицинских журналов за последние шестнадцать лет, используя ключевые слова: арктический, полярный круг, диета, Омега 3, сезонные нарушения и суициды. Кроме того, были использованы архивы Университета Аляски и публикации, отсутствующие в электронном формате. Полученные данные говорят о значительном увеличении воспалительных заболеваний у народов, проживающих за полярным кругом, питание которых за короткий срок изменилось с пищи с высоким содержанием жирных кислот Омега 3 на использование западной диеты. (McGrath-Hanna NK et al. 2003).
3 – ПРЕИМУЩЕСТВА ДИЕТ, СОДЕРЖАЩИХ ЖИРНЫЕ КИСЛОТЫ ОМЕГА-3
Итак, все перечисленное выше это теория. Мы поменяли наше питание, не имея времени для адаптации к нему, и это свершившийся факт. Перемена питания в значительной степени связана с типом потребляемых жиров, а у народов, которые поменяли диету в течение одного поколения, показатель воспалительных заболеваний увеличился особенно резко. Также существует возможное биохимическое объяснение: изменения фосфолипидов в клеточных мембранах и перкурсоров PG могут стать причиной образования воспалительных PG. Следует добавить, что на воздействие на каскад воспалительных медиаторов, производных арахидоновой кислоты, добавка в рацион Омега-3 оказывает различное влияние, т.к. было доказано, что эти кислоты действуют на провоспалительные цитокины, изменяя экспрессию генов (Рис. 6). Противовоспалительное действие может быть обусловлено наличием антагонизма с производными АА или прямо вызывать межклеточный сигнал, которые активирует фактор транскрипции как ядерный фактор каппа В (NFB) или оба фактора. По этому поводу имеются недавние исследования, которые доказывают, что жирные кислоты Омега-3 могут регулировать в сторону понижения активность NFB, улучшая симптомы таких хронических воспалительных заболеваний, как ревматоидный артрит или астма (Calder PC 2002).
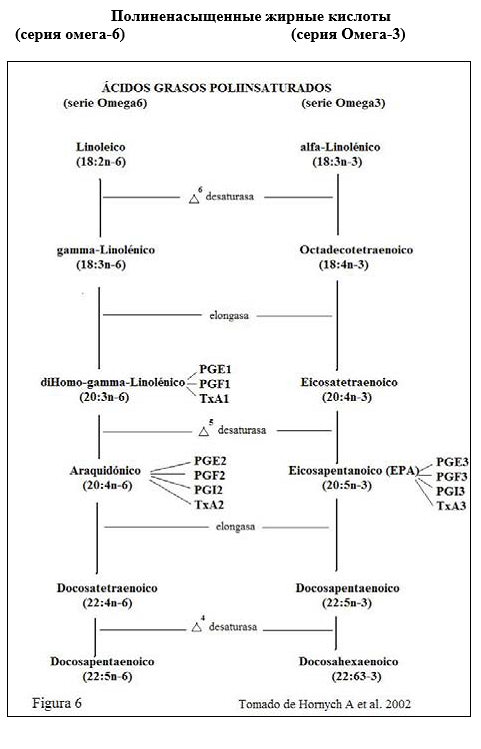
Другие благоприятные свойства Омега 3 включают уменьшение плазматических триглицеридов и агрегацию тромбоцитов, а также изменение равновесия в балансе эйкозаноидов в пользу сосудорасширяющих. Кроме того, сокращают возбуждение миоцитов и артериальное давление в ответ на гормональное стимулирование. (Weber C et al/ 1995).
Ответим на вопросы, которые мы поставили в начале статьи.
1. Потребляемые жирные кислоты должны достичь мембран и мест, где происходят физиологические процессы. Это должно быть подтверждено прямыми или косвенными методами, в случае если последние невозможны.
В замечательной работе Kim HK и Choi H приводится исследование, проводившееся на крысах, которым назначили 5 диет, различающихся по пропорции и типам жиров, с последующим измерением постпрандиального липидного уровня и его состава в мембранах гепатоцитов.
- диета 1: без жиров
- диета 2: с добавлением 10% (от веса) жира кукурузного масла
- диета 3: с добавлением 10% (от веса) жира телятины
- диета 4: с добавлением 10% (от веса) жира периллового масла (perilla frutescens) с соотношением Омега3/Омега 6 - 3/1.
- диета 5: с добавлением 10% (от веса) жира рыбы.
Исследования проходили на группах крыс в течение 4 недель и еще в течение 4 дней, чтобы проверить результат в зависимости от времени питания.
Первый результат состоял в том, что плазматические липиды менялись в зависимости от потребленного жира. Плазматические и печеночные триглицериды и общий холестерин понизились на 4 и 5 во 2 и 3 диетах. Состав жирных кислот мембраны гепатоцитов адаптировался к изменению питания. Состав жирных кислот у крыс, которым назначалась диета 3, имел существенное превышение пальметиновой, стеариновой и олеиновой кислоты. У крыс, которым назначали диету 2 повысилась линоевая и арахидоновая кислоты, в 4 диете - альфа-линоленовая и ЕРА и в 5 диете – пальметиновая кислота и DHA.
Оба эксперимента, проводившиеся как в течение 4 недель, так и 4 дней, показали одинаковые результаты. Кроме того, уровни общих печеночных липидов имели отрицательную корреляцию с содержаниями DHA и EPA.
На рис. 7 представлен путь, которым могут следовать жирные кислоты (AG), получаемые из жировой ткани или липопротеинов после их приема с пищей.
После проникновения через плазматическую мембрану при помощи транспортера (FAT) жирные кислоты могут использоваться для синтеза триглицеридов или могут быть подвергнуты действию элонгаз, десатураз или участвовать в получении энергии или в синтезе простагландинов, тромбоксанов или лейкотриен.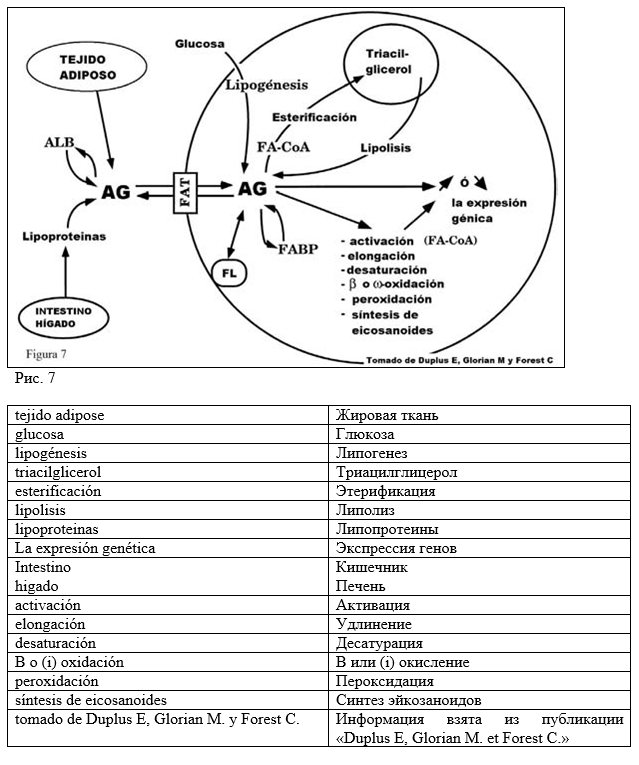
И наконец, AG модулирует (положительно или отрицательно) транскрипцию одного чувствительного гена, кодируя транспортный белок или метаболизм AG (Duplus et al. 2000).
2. Должны модифицировать концентрации простагландинов, тромбоксанов и лейкотриен, вызывающих воспаление, что также следует измерить, по возможности, прямыми методами.
Было проведено исследование на мышах, для которых использовали диеты, обогащенные Омега-3; отмечались понижения синтеза лейкотриен серии 4 (SP-LT) (LTC4 и LTE4) до 76% в сравнении с мышами, которым была назначена контрольная диета, а также синтез 6-цето-простагдандина F1 альфа понизился на 81% у мышей, которым назначили диету, содержащую соотношение n3/n6 1.93, в то время как синтез простагландинов Е2 сократился на 44% (Broughton KS et al. 1991).
Благодаря достижениям в магнитно-резонансной томографии нам известно, что незначительные изменения в степени восстановления фосфолипидов устанавливают различия в перемещении и проходе передатчиков через биомембраны. (Salem NJr et al. 2001), а также напомним, что полиненасыщенные кислоты диеты вовлечены в регулирование генной экспрессии стерола-регулятора, который связывает протеин-1 (SREBP-1 (sterol regulatory element-binding protein-1), который играет ключевую роль в регулировании синтеза липидов, их окисления и термогенеза (Price PT, et al. 2000).
3. Клинические исследования должны подтвердить данную метаболическую гипотезу (эксперименты на животных и людях).
Множество авторов (проверка, выполненная Brown AA and Hu FB 2001), которые нашли связь между отношением Омега-6/Омега-3 и заболеваниями эндотелия сосудов (атеросклероз > ишемическая кардиомиопатия), хотя наиболее ясные результаты представлены в исследованиях Inuit (Dewailly E et al 2001).
В других исследованиях продемонстрировано, что потребление рыбьего жира, похоже, приводит к снижению сужения бронхов, вызванного интенсивными аэробными упражнениями элитных спортсменов (Mickleborough TD et al. 2003).
Другие исследования демонстрируют противовоспалительное и иммуннорегулирующее действие жирных кислот Омега-3 (Calder PC 1998), а также благотворное действие на сердечную деятельность. (Kromhout D et al 1985).
И наконец, похоже, что эйкозапентаеновая кислота имеет большие противовоспалительные свойства по сравнению с DHA, а также выступает как антиагрегант тромбоцитов (Hirai A et al 1989) (Lee TH et al.1991).
Какое количество жирных кислот Омега-3 следует употреблять? Возможно следует просто увеличить количество потребляемой рыбы?
Ежедневно необходимо употреблять 350-400 мг/день (0,4% от общего количества Ккал) (FAO, 1997). Хотя отмечается некоторое улучшение состояния больных, которым назначается диета с большим количеством жирной рыбы, тем не менее, мы не можем говорить об увеличении рыбной диеты больным, т.к. это означает насилие над метаболическими путями; к тому же терапевтические количества ЕРА и DHA можно получить только посредством добавки в рацион 2 г/день докозагексаеновой кислоты (DHA) (Horrobin D, 2003). Напомним, что у человека переход альфа-линоленовой кислоты (ALA) в ЕРА (?-6-десатураза) ограничен, в результате прием ALA приводит только к незначительному увеличению ЕРА, но совершенно не увеличивает DHA.
Имеются ли противопоказания для приема ЕРА?
Похоже, что нет. Необходимо только осторожно назначать больным, которые принимают антикоагулянты, хотя в некоторых исследованиях отмечается незначительное иммуноугнетающее действие, которое еще необходимо проверить. (Wu D et al. 1999; Thies F et al. 2000).
Чтобы достичь доз, которые успешно применялись в различных проанализированных исследованиях, нужно принимать капсулы рыбьего жира с богатым содержанием эйкозапентаеновая и докозагексаеновой кислоты, т.к. простое употребление рыбы не приводит к показателям, необходимым для изменения экспрессии генов.
Выпускаемые в продажу жирные кислоты Омега-3 получают из различных видов рыбы: сельди, семги, сардин, тунца, скумбрии, ставриды. Торговые марки в нашей стране, выпускающие эти продукты: Vigor EPA ® с содержанием ЕРА 18% и DHA 12%; Ergy 3 ® THF 18% и DHA 12%.
И наконец, новое и обещающее соединение, похоже, может усилить противовоспалительное действие традиционной терапии. Новые исследования показали, что DHA может произвести докозатриены, новые биологически активные медиаторы, которые благодаря активности лейкоцитов могут трансформировать 17-HDHA и превращать его в резолвины (Рис. 8) – вещества имеющее непосредственное отношение к воспалительному феномену (Hong S et al 2003), причем аспирин, который действует на уровне СОX-2 благоприятствует появлению резолвинов (Serhan CN et al. 2002).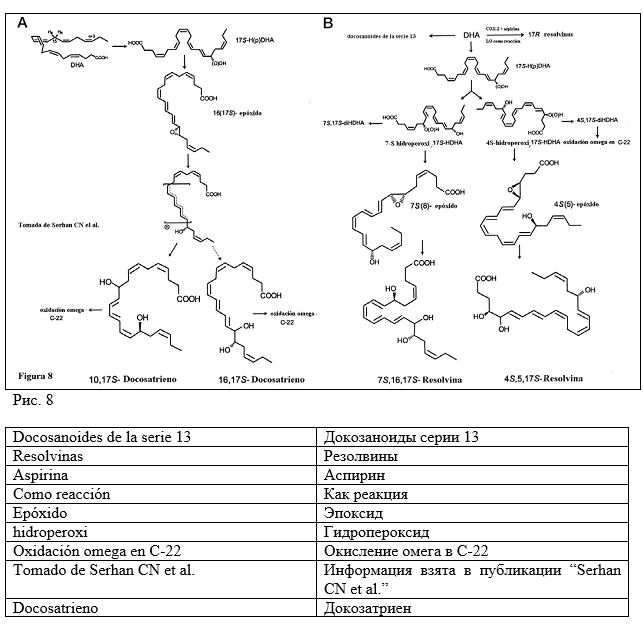
АВТОРЫ
Хосе Антонио Вильегас Гарсия
Мария Тереза Мартинес Рокамора
Франсиско Хавьер Лопес Роман
Ана Белен Мартинес Гонсалес
Антонио Хосе Луке Рубия
МЕСТО РАБОТЫ
Кафедра физкультурной физиологии
Католического университета Мурсии


